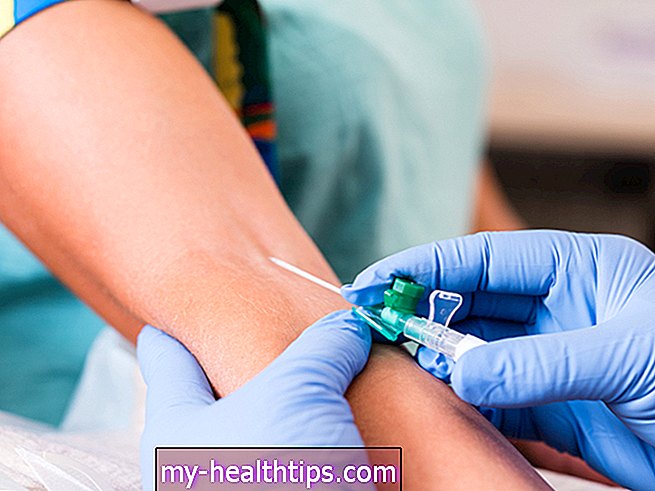
Estou usando o novo monitor de glicose contínuo implantável Eversense desde o início de dezembro e publiquei uma análise inicial completa do produto aqui.
Três meses depois, com meu desgaste de 90 dias chegando ao fim, tive a opção de continuar implantando um novo sensor ou não. Escolhi sim, com base na precisão, confiabilidade e - não insignificantemente - na maravilhosa trégua que esse sistema me dá do cansaço do alarme.
Hoje, gostaria de compartilhar algumas das minhas experiências pessoais adicionais e também algumas atualizações oficiais sobre este novo sistema CGM - incluindo como conseguir ajuda para pagar por ele e onde me voluntariar para ensaios clínicos.
Esse alerta de “luz ambiente” Eversense
Quando fui inserido pela primeira vez com Eversense, lembro-me de alguma menção superficial de um problema com luz brilhante. Mas não foi enfatizado e realmente não ganhou vida para mim até que eu tirei meus suéteres de inverno para comprar equipamento de caminhada em Palm Springs, algumas semanas atrás.

O momento foi infeliz, pois eu superestimei os carboidratos do café da manhã e atingi um nível baixo no momento em que estávamos saindo para nossa primeira caminhada do fim de semana. Lá estávamos nós nas colinas áridas queimadas pelo sol acima de Palm Desert, comigo engolindo skittles e checando o aplicativo Eversense a cada poucos minutos, quando de repente recebi uma nova mensagem de erro nunca vista antes: "High Ambient Light". Huh?
Aparentemente, "Nenhuma leitura de glicose pode ser exibida até que a luz ambiente seja reduzida." Não é um momento feliz na trilha de caminhada - Ack!
Tudo que eu conseguia pensar era: “Essa coisa não funciona na luz solar direta, que diabos ?!”
Eu pesquisei mais tarde online e fui lembrado de que todo o sistema Dang é construído na luz.
“O Sensor Eversense é um fluorômetro miniaturizado patenteado que usa intensidade fluorescente para medir a glicose no fluido intersticial ... Um diodo emissor de luz embutido no sensor excita o polímero, e o polímero então sinaliza rapidamente as mudanças na concentração de glicose por meio de uma mudança na saída de luz.”
Também falei com a cientista-chefe sênior da Senseonics, Carrie Lorenz, que explicou o alerta de “High Ambient Light” da seguinte maneira:
“Pense nisso como sentar ao redor de uma fogueira e alguém iluminar seus olhos com uma lanterna. É muito forte e por um minuto você não consegue ver mais nada ... É um mecanismo de segurança embutido em nosso algoritmo que basicamente diz, esta luz é muito brilhante e está bloqueando a capacidade de ver a luz que importa, que está relacionada à glicose . ”
Ela também explicou que esse alerta vai “leitura por leitura, a cada 5 minutos”, o que significa que as leituras de glicose devem começar a aparecer novamente alguns minutos após a remoção da área brilhante.
O Guia de início rápido da Senseonics sugere:
“Se você receber um alerta de luz ambiente (mais comum no uso precoce), tente se afastar da luz direta, cobrindo o transmissor inteligente com roupas mais escuras ou colocando o transmissor inteligente ligeiramente mais alto no braço sobre o sensor.”
Observe que o problema é com o sensor implantado e não com o transmissor preto usado do lado de fora, então uma dica que recebi é que, se você sabe que estará sob luz forte, pode simplesmente dobrar os adesivos brancos para dar o sensor mais sombra.
Quando eu tuíte sobre a interferência da luz ser uma grande desvantagem em potencial, um usuário experiente do Eversense respondeu:
“Não é, na minha experiência, que o alerta é apenas um aviso, não afeta realmente a precisão. Além disso, você sempre pode usar um adesivo / fita adesiva colorida para cobrir o local do sensor e está tudo bem. Não é grande coisa :)"
Te peguei, mas ainda é algo para se manter em mente se você mora em um lugar ensolarado.
Minha segunda inserção
No início de março, voltei ao consultório do meu médico para remover o sensor Eversense do meu ombro esquerdo e inserir um novo no direito.
Disseram-me que o médico iria começar com a inserção primeiro, especificamente para manter tudo ultra-esterilizado: "trabalho limpo antes do trabalho 'sujo' de remover uma substância de seu corpo." Entendi.
Fui coberto novamente com uma cortina cirúrgica, anestesiado, e o procedimento foi rápido e suave, sem dor.
Em seguida, virei e a cortina e a injeção anestésica foram aplicadas no meu ombro esquerdo. Eu esperava um procedimento igualmente rápido e fácil, mas infelizmente não foi assim. Esta foi, aparentemente, a primeira remoção do meu médico em um paciente real - ela estava praticando profusamente com aqueles braços protéticos - e ela simplesmente não conseguia agarrar o minúsculo sensor com a braçadeira fornecida. Entorpecido como eu estava, parecia apenas um monte de cutucadas e cutucadas irritantes, mas depois de alguns longos minutos, a posição ficou bem desconfortável. Meu pescoço estava rígido e eu estava começando a ficar preocupado com cicatrizes no meu ombro (o que a equipe me garantiu que não deveria ser o caso, já que a incisão continua minúscula). De qualquer forma, eles finalmente desistiram e me remendaram com o sensor ainda lá.
Sim, você leu certo: eles não conseguiram tirar o sensor. É claro que ele pode ser removido posteriormente, depois que meu braço estiver curado e pronto para uma nova tentativa.
E sim, o pensamento de que ficou preso lá meio que me assustou no início. Os especialistas da Eversense me garantiram que, mesmo que o sensor ficasse em um corpo pelo resto da vida, não faria mal, pois é feito de plástico biocompatível super seguro.
“Quando começamos a desenvolver o Eversense, tivemos que decidir em que encaixar os componentes eletrônicos ... Encontramos esse plástico chamado polimetilmetacrilato (pmma) que ficou embutido nos corpos de vários veteranos da Força Aérea da Segunda Guerra Mundial depois que seus aviões explodiram. Eles tinham peças neles por anos sem nenhuma reação ”, me diz o cientista da Eversense Lorenz.
Ela observa que esse plástico agora é “universalmente comum” e até mesmo documentado como seguro para uso cosmético.
OK, mas ainda me encolhi um pouco quando vim e disse à minha filha, "eles não conseguiram tirar" e sua resposta foi simplesmente, "Ewwww.”
Não estou compartilhando isso para assustar ninguém - é simplesmente minha experiência, que a equipe da Eversense me disse que é bastante rara.
Também soube que eles estão atualmente realizando um treinamento de remoção de sensor em Las Vegas e em outros lugares, ensinando os médicos a encontrar o sensor usando ultrassom, marcá-lo e removê-lo de forma rápida e eficiente. Bom ouvir.
Integração Glooko-Eversense
Você já ouviu falar que o pessoal da Eversense anunciou a integração com a plataforma Glooko D-data? Isso significa que se você baixar o aplicativo Glooko no seu telefone, agora você pode simplesmente escolher o ícone “Eversense” para vincular ao seu sensor ao vivo, onde você pode visualizar conjuntos de dados de 1 semana, 2 semanas, 1 mês e 3 meses .
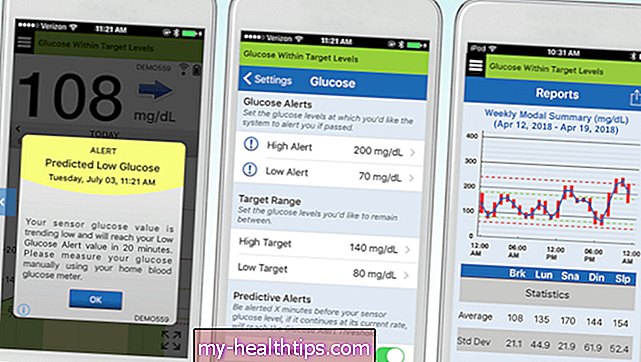
Isso é especialmente legal para usuários de Omnipod (bomba de insulina tubeless) como eu, já que esse dispositivo também é configurado para fácil integração com o Glooko.
Agora posso ver minhas médias CGM ao lado da média de insulina por dia, tempo na faixa-alvo e porcentagem de altos e baixos. Ao clicar em “Ver mais”, você também pode obter detalhes e até mesmo dividir essas informações por dia. Estou animado para revisar essas informações com meu médico em breve, já que nunca tive acesso a CGM e dados de dosagem de insulina lado a lado antes.
Dr. Fran Kaufman entra para a Eversense
Parabéns à empresa por trás da Eversense, Sensionics, de Maryland, por prender provavelmente o diretor médico mais procurado no mundo do diabetes: Dr. Fran Kaufman, que “se aposentou” como CMO da Medtronic há apenas três meses, em dezembro de 2018.

Na época, ela disse que queria se concentrar em seu hobby de escrever e passar mais tempo com sua família. Não se pode deixar de imaginar se ela já estava em contato com a Senseonics sobre oportunidades lá.
Afinal, os dispositivos D implantáveis sempre foram uma paixão dela, desde a bomba de insulina implantável que a Medtronic estava trabalhando, mas abandonada em 2011. (Veja a pesquisa improvisada que fizemos na época, perguntando aos pacientes se eles seriam receptivos a um dispositivo implantável.)
Esse dispositivo ficou disponível por um curto período na França, mas de acordo com Kaufman, era “difícil de adotar” e a formulação de insulina concentrada necessária para fazê-lo funcionar “ainda estava sendo desenvolvida e refinada”.
“É um dispositivo complexo que requer atenção e cuidados meticulosos. Reabastecer e reajustar é um desafio. Estamos trabalhando para tornar a bomba menor e mais fácil de adotar ”, escreveu ela na época.
Agora, tendo defendido o primeiro sistema híbrido de loop fechado na Medtronic, Kaufman tem a oportunidade de retornar ao sonho implantável com a Eversense.
Sua declaração no comunicado de imprensa, sem nenhuma surpresa, dizia:
“Estou muito animado para me juntar à equipe Senseonics, especialmente neste ponto onde sinto que tenho a oportunidade de ajudar a estabelecer as bases para o primeiro sistema de monitoramento contínuo de glicose implantável de longo prazo.
Como observado, parabéns à nova Sensionics por prender um médico veterano tão respeitado e especialista em tecnologia médica!
“Programa de ponte” para compensar negações de seguro
Em seu Earnings Call na última terça-feira, a Senseonics revelou um novo “Programa de Ponte de Acesso ao Paciente” para ajudar a superar atrasos na cobertura de seguro para este novo sistema.
Observe que isso é apenas para pessoas com seguro e não está disponível para pacientes do governo ou qualquer pessoa que more no estado de Massachusetts devido a restrições específicas lá.
Funciona assim:
O vice-presidente e GM dos Estados Unidos Mike Gill explica que, embora centenas de pacientes segurados já estejam trabalhando com seus médicos para entrar no Eversense, eles enfrentam a recusa de cobertura por cinco das principais seguradoras do país, que projetaram erroneamente o sistema como “E / I ”também conhecido como experimental / investigacional:
- Unidos
- Cigna
- Humana
- Hino
- HCSC (Blue Cross Texas, Illinois, Novo México, Oklahoma, Montana)
“Embora tivéssemos um painel completo de aprovação do FDA, eles colocaram o rótulo 'E / I' (Eversense), portanto, atualmente não estão cobrindo isso”, diz Gill.
Para combater isso, o novo Programa Bridge oferece basicamente aos pacientes uma taxa fixa de US $ 99 para todos os suprimentos iniciais - sensor, transmissor, adesivos, guia inicial - que normalmente custaria cerca de US $ 1400.
Os pacientes ainda terão que pagar pelo procedimento de inserção de acordo com a taxa de seu médico (geralmente em torno de US $ 200).
Portanto, alguém coberto pelo United e que tenha o pedido negado, por exemplo, acabaria pagando apenas US $ 299 pelo dinheiro todo. Outras seguradoras como a Aetna ainda podem exigir um copagamento de 20% sobre os suprimentos além dos US $ 99, mas este Programa Bridge coloca o preço total no mesmo nível de outros sistemas CGM, diz Gill.
Ele lembra ainda que a empresa não pode subsidiar o procedimento de inserção em si, pois isso seria visto como “indução” ilegal dos médicos a prescreverem determinado sistema. “O que podemos fazer é ajudar os pacientes com os custos de abastecimento”, diz ele.
Ensaios clínicos Eversense e expansão do uso
A Eversense tem vários estudos em andamento na Europa atualmente e nos EUA está recrutando pacientes para seu estudo principal PROMISE que reunirá evidências para a aprovação do uso em 180 dias (em oposição aos 90 dias atuais). Os locais de teste estão na Califórnia, Geórgia, Texas e no estado de Washington.
Observe que você pode se voluntariar para esse estudo ao longo dos próximos meses, mas precisa ser um adulto já trabalhando com seu médico no Eversense; eles não estão apenas fornecendo sensores gratuitos para qualquer um que dê um passo à frente.
No front loop fechado, eles concluíram um estudo com o sistema iLet Bionic Pancreas sendo desenvolvido pela Beta Bionics - um estudo de viabilidade multicêntrico usando Eversense pela primeira vez em um sistema AP. Dezoito pessoas participaram desse estudo e planejam revelar os resultados nas grandes ADA SciSessions anuais em junho de 2019.
O chefe de vendas Gill nos disse que a empresa submeteu sua revisão da FDA para a designação "não-injuntiva" - a cláusula afirmando que um CGM é preciso o suficiente para uso de dosagem sem testes de punção digital como backup. Eles estão esperando por esta "alegação de dosagem" no primeiro trimestre de 2020.
Eles também estão avaliando maneiras de tirar aquele transmissor preto dos ombros das pessoas (!)
Um "Estudo da Casa" concluído até agora na Romênia analisou o desgaste no abdômen em comparação com a parte superior do braço (não seria bom ?!). A empresa espera apresentar um pôster de pesquisa sobre a preferência do paciente também na grande reunião da ADA em junho.
Mas algumas pessoas não estão testando sites alternativos "off-label"? nós perguntamos.
Gill basicamente diz que o fabricante não está fiscalizando isso. Na verdade, em seu estudo de pós-aprovação para o sensor de 90 dias, “se um médico decidir não usar o rótulo, pedimos apenas que ele registre essa informação”.
E embora eles não estejam recrutando especificamente para esse propósito, no estudo de pós-aprovação eles também estarão registrando experiências de pacientes com diferentes tipos de pele - afro-americanos, latino-americanos e PCDs brancos. (Pense no problema da luz ambiente, mencionado acima).
A Senseonics diz que atualmente tem 60 milhões de "vidas cobertas", ou seja, pacientes segurados que têm acesso ao Eversense nos EUA, e tem uma meta de chegar a 100 milhões até o final de 2019. Mais de 250 médicos prescreveram prescrições para o Eversense CGM, e eles espero expandir o uso, certificando enfermeiros e assistentes médicos nos EUA e na Europa para inserir e dar suporte ao sistema.
Estou satisfeito por estar entre a primeira maioria.
{ISENÇÃO DE RESPONSABILIDADE: nas próximas semanas, farei um trabalho limitado de consultoria para a Senseonics, sendo compensado para fornecer feedback detalhado do usuário.}
















-what-you-need-to-know.jpg)